[ ]ক্ষার এবং ক্ষারকের পার্থক্য ||ক্ষার ও ক্ষারকের মধ্যে পার্থক্য
ক্ষার এবং ক্ষারকের মধ্যে পার্থক্য
নিম্নে ক্ষার ও ক্ষারকের মধ্যে পার্থক্য প্রদান করা হল:
🎷পার্থক্য-১:
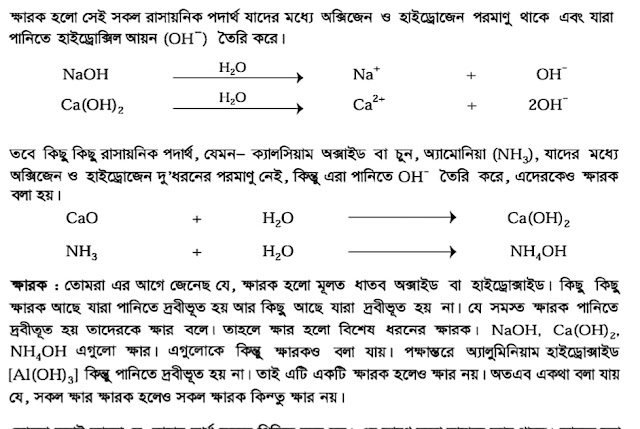
ক্ষারক হলাে মূলত ধাতব অক্সাইড CaO বা হাইড্রোক্সাইড [NaOH, KOH, Ca(OH)₂, Al(OH)₃ ] ।ক্ষারক এসিডের সাথে বিক্রিয়া করে লবণ ও পানি উৎপন্ন করে।
NaOH একটি ক্ষারক ,কারণ এসিডের সাথে বিক্রিয়া করে লবণ পানি উৎপন্ন করে। বিক্রিয়াটি নিম্নরূপ:
NaOH +HCl = NaCl +H₂O
এখানে,
●NaOH =ক্ষারক
●HCl =এসিড বা অম্ল
●NaCl = লবণ
●H₂O =পানি
এবার কথা হল ,কিছু কিছু ক্ষারক আছে যারা পানিতে দ্রবীভূত হয় না আর কিছু ক্ষারক আছে যারা দ্রবীভূত হয় ।
যে সব ক্ষারক(Base) পানিতে দ্রবীভূত হয়, তাদেরকে বলে ক্ষার বা অ্যালকালি(Alkali)। তাহলে বোঝা যাচ্ছে যে, ক্ষার হতে গেলে ক্ষারক কে(Base)অবশ্যই পানিতে দ্রবীভূত হতে হবে।
২)ক্ষারক পানিতে দ্রবীভুত হতেও পারে বা নাও হতে পারে। কিন্তু, ক্ষার পানিতে দ্রবীভুত হবেই।
পার্থক্য-২:
ক্ষার হলাে বিশেষ ধরনের ক্ষারক।
সকল ক্ষারই ক্ষারক কিন্তু সকল ক্ষারক ক্ষার নয়
ক্ষার এবং ক্ষারকের মধ্যে পার্থক্যর উদাহরণ:
NaOH, KOH, Ca(OH)₂ এরা সবাই ক্ষার এবং ক্ষারক (উভয়)। কারণ এরা দুটি শর্ত পালন করে।
এক,
এরা এসিডের সাথে বিক্রিয়া করে লবণ পানি উৎপন্ন করে।
দুই, এরা পানিতে দ্রবীভূত হয়।
অপরদিকে, অ্যালুমিনিয়াম হাইড্রোক্সাইড, Al(OH)₃ , একটি ক্ষারক কিন্তু অ্যালুমিনিয়াম হাইড্রোক্সাইড পানিতে দ্রবীভূত হয় না। যেহেতু অ্যালুমিনিয়াম হাইড্রোক্সাইড পানিতে দ্রবীভূত হয় না, সেহেতু ক্ষার হওয়ার শর্ত অ্যালুমিনিয়াম হাইড্রোক্সাইড পূরণ করতে ব্যর্থ ।তাই অ্যালুমিনিয়াম হাইড্রক্সাইড একটি ক্ষারক হলেও ক্ষার নয়।
আবার CuO একটি ক্ষারক কিন্তু ক্ষার নয় ।
ক্ষারক পানিতে দ্রবীভুত হতেও পারে বা নাও হতে পারে। কিন্তু, ক্ষার পানিতে দ্রবীভুত হবেই।
CO2 এর লুইস ডট চিত্র
আরো পড়ুন:

Comments
Post a Comment